

Símbolo
Zn
Nombre: Zinc
Número Atómico: 30
Masa Atómica: 65.409

Estado de agregación: Sólido
Punto de ebullición, °C: 907
Punto fusión, °C: 420
Electronegatividad: 1.7
Estados Oxidación: +2
Configuración electrónica: [Ar]3d104s2
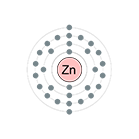
Metal más abundante en la Tierra, presenta color blanco y azulado que se empaña en el aire.
Conduce la electricidad.
Si bien puede ser un metal frágil, a una temperatura aproximada de entre 100° y 150°C se vuelve maleable, tiene propiedades súper plásticas y a unos 238°C logra propiedades ferromagnéticas.
Se obtiene de sus minerales zinc blende (sulfuro de zinc) y la calamina (silicato de zinc), por tostación para obtener el óxido de zinc y posterior reducción a zinc metálico mediante calentamiento con carbono o por electrólisis.

Para el galvanizado de hierro, usado en carrocerías, farolas, barreras de seguridad y puentes colgantes.
En aleaciones como latón, níquel plata y soldadura de aluminio.
En la fabricación de pilas secas.
En fundiciones, que son importantes en la industria del automóvil, la industria eléctrica y de hardware.
Algunos de sus compuestos se usan en la fabricación de pinturas, caucho, cosméticos, productos farmacéuticos, plásticos, tintas, jabones, baterías, textiles y equipo eléctrico, pinturas luminosas, luces fluorescentes y pantallas de rayos X.

No se conoce quien lo descubrió, ni en qué lugar y año, sin embargo, ya era conocido desde la antigüedad.
Proviene de la palabra alemana "zink" nombre con el que se designaba a uno de los metales presentes en el latón (aleación de cobre y zinc) o también de la palabra alemana "zinke" (punta aguda) por la forma que adoptaba al depositarse en los altos hornos.
Se conocen aleaciones de zinc desde el 1400 y el 1000 a. C.
El zinc metálico se obtuvo en el siglo XIII en la India mediante reducción de calamina (carbonato de zinc) con sustancias orgánicas, y en 1746, Andreas Marggraf utilizó carbón.